10 .G.viii. Ambidentní substráty
Některé substráty (např. 1,3-dichlorbutan) mohou být napadeny na dvou nebo více pozicích a lze je nazvat ambidentní substráty . V uvedeném příkladu jsou to v molekule dvě odstupující skupiny. Kromě dichlorbutanu obecně existují dva druhy substrátů, které jsou ve své podstatě ambidentní (pokud nejsou symetrické). Jeden z nich, allylový typ, již byl diskutován (kap. 10. E). Druhým je epoxidový (nebo podobný aziridin nebo episulfidový) substrát. 525 Selektivita pro jednu nebo druhou pozici se obvykle nazývá regioselektivita.
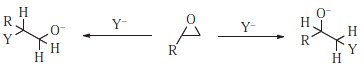
Substituce volným epoxidem, ke kterému obvykle dochází za základních nebo neutrálních podmínek, obvykle zahrnuje mechanismus S N 2. Protože primární substráty jsou podrobeny napadení S N 2 snadněji než sekundární, nesymetrické epoxidy jsou napadány v neutrálním nebo bazickém roztoku na méně vysoce substituovaném uhlíku a stereospeciálně s inve Za kyselých podmínek je reakcí podroben protonovaný epoxid. Za těchto podmínek může být mechanismem buď S N 1 nebo S N 2. V S N 1 mechanismech, které upřednostňují terciární uhlíky, může útok lze očekávat na silněji substituovaném uhlíku, a je tomu skutečně tak. I když však protonované epoxidy reagují tím, co se očekává jako mechanismus S N 2, útok je obvykle na silněji substituovaném uhlíku. substituovaná poloha. 526 Tento výsledek pravděpodobně naznačuje významný karbokační charakter na uhlíku (například párování iontů). Je tedy často možné změnit směr otevírání kruhu změnou podmínek z bazického na kyselý nebo naopak.
Při otevření kruhu 2,3-epoxidových alkoholů zvyšuje přítomnost $ \ ce {Ti (O \ textit iPr) 4} $ rychlost i regioselektivitu , upřednostňující útok na C-3 spíše než na C-2. 527 Když je epoxidový kruh fúzován s cyklohexanovým kruhem, otevření kruhu S N 2 vždy dává spíše diaxiální než diequatoriální otevření kruhu. 528
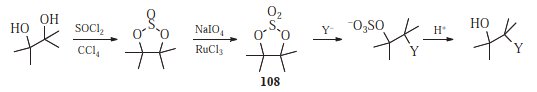
Cyklické sulfáty ( 108 ), připravené z 1,2-diolů, reagují stejným způsobem jako epoxidy, ale obvykle více rychle: 529
524 Chechik, VO; Bobylev, V.A. Acta Chem. Scand. B , 1994 , 48, 837.
525 Rao, A.S .; Paknikar, S.K .; Kirtane, J.G. Tetrahedron 1983 , 39, 2323; Behrens, C.H .; Sharpless, K.B. Aldrichimica Acta 1983 , 16, 67; Enikolopiyan, N.S. Čistá aplikace Chem. 1976 , 48, 317; Dermer, O.C .; Ham, G.E. Ethylenimine and Other Aziridines , Academic Press, NY, 1969 , str. 206–273.
526 Biggs, J .; Chapman, N.B .; Finch, A.F .; Wray, V. J. Chem. Soc. B 1971 , 55.
527 Caron M .; Sharpless, K.B. J. Org. Chem. 1985 , 50, 1557. Viz také Chong, J.M .; Sharpless, K.B. J. Org. Chem. 1985 , 50, 1560; Behrens, C.H .; Sharpless, K.B. J. Org. Chem. 1985 , 50, 5696.
528 Murphy, D.K .; Alumbaugh, R.L .; Rickborn, B. J. Dopoledne. Chem. Soc. 1969 , 91, 2649. Metodu přepsání této preference viz McKittrick, B.A .; Ganem, B. J. Org. Chem . 1985 , 50, 5897.
529 Gao, Y .; Sharpless, K.B. J. Dopoledne. Chem. Soc. 1988 , 110, 7538; Kim, B.M .; Sharpless, K.B. Tetrahedron Lett. 1989 , 30, 655.